cs2,so2,NH3熔沸点怎么比
编辑:huantt 成考报名 发布时间:03-23 阅读:
物质的熔点(melting point),即在一定压力下,纯物质的固态和液态呈平衡时的温度,也就是说在该压力和熔点温度下,纯物质呈固态的化学势和呈液态的化学势相等,而对于分散度极大的纯物质固态体系(纳米体系)来说,表面部分不能忽视,其化学势则不仅是温度和压力的函数,而且还与固体颗粒的粒径有关,属于热力学一级相变过程。以下是中国招生考试网www.chinazhaokao.com 分享的cs2,so2,NH3熔沸点怎么比,希望能帮助到大家!
·2015年浙江义乌中考化学试卷及答案(完整版)[1](2015-07-05)
·2015年广东中考化学试题及答案(已公布)[1](2015-07-05)
·2015年湖北荆州中考化学试卷及答案(完整版)[1](2015-07-05)
·2015年浙江义乌中考化学试题及答案(已公布)[1](2015-07-05)
·2015年广东揭阳中考化学试卷及答案(完整版)[1](2015-07-05)
·2015年广东揭阳中考化学试题及答案(已公布)[1](2015-07-05)
cs2,so2,NH3熔沸点怎么比
关于CS2、SO2、NH3三种物质的说法中正确的是[AB ]
A.CS2在水中的溶解度很小,是由于CS2属于非极性分子
B.SO2和NH3均易溶于水,原因之一是它们都是极性分子
C.CS2为非极性分子,所以在三种物质中熔沸点最低
D.NH3在水中溶解度很大只是由于NH3分子有极性
溶解性:
(1)相似相溶原理:极性分子易溶于极性分子溶剂中(如HCl易溶于水中),cs2,so2,NH3熔沸点怎么比非极性分子易溶于非极性分子溶剂中(如CO2易溶于CS2中)
(2)分子结构:含有相同官能团且该官能团在分子中所占比重较大的物质能够相互溶解。如:乙醇与水互溶;戊醇不能与水互溶、与己烷能互溶。
(3)分子之间能形成氢键,会增大溶解度。
(4)溶质若能与溶剂发生反应,溶解度会增大。
影响物质溶解性的因素:
1.看溶质与水能否发生反应
溶质若能与水发生反应,则会增大溶质的溶解度,如
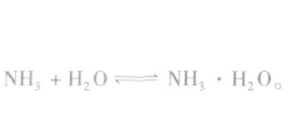
2.分子的极性
非极性分子构成的物质易溶于非极性溶剂,难溶于极性溶剂;极性分子构成的物质易溶于极性溶剂,难溶于非极性溶剂。如苯易溶于植物油而难溶于水; NH3、HCl易溶于水而难溶于苯。
3.氢键
溶质与溶剂分子之间若能形成分子问氢键,会增大溶质的溶解度。如NH3、HF都能与H2O形成分子间氢键,溶解度较大。
●【往下看,下一篇更精彩】●
